💠 고체 NaCl을 액체로 용융시키는 데 필요한 에너지는? 💠
고체 상태의 **NaCl(염화나트륨)**을 녹여 **액체 상태(용융 상태)**로 만들 때 필요한 에너지는 융해 엔탈피(Heat of Fusion, ΔH_fus) 또는 **융해열(Latent Heat of Fusion)**이라고 합니다.
---
🔷 융해 엔탈피(Heat of Fusion, ΔH_fus)란?
✔ 정의:
고체를 녹여 액체로 변환하는 데 필요한 에너지입니다.
고체 상태의 입자들은 강한 정전기적 인력으로 결합되어 있지만, 온도를 올리면 입자들의 운동 에너지가 증가하여 결합이 부분적으로 깨지며 액체로 전환됩니다.
이 과정은 흡열 반응(endothermic reaction) 이므로 양수(+) 값을 가집니다.
✔ NaCl의 융해 엔탈피
NaCl의 융해 엔탈피(ΔH_fus) ≈ +27 kJ/mol
즉, 고체 NaCl을 액체 NaCl로 변환하려면 27 kJ/mol의 에너지를 공급해야 합니다.
---
🔷 NaCl 용융 반응식
📌 고체 → 액체 전환 과정:
NaCl(고체) + 27 kJ/mol → NaCl(액체)
✔ 이 과정은 흡열 반응이므로 에너지를 가해야 합니다.
📌 NaCl이 다시 고체로 응고될 때:
NaCl(액체) → NaCl(고체) + (-27 kJ/mol)
✔ 응고(결정화) 과정에서는 에너지가 방출되며 발열 반응입니다.
---
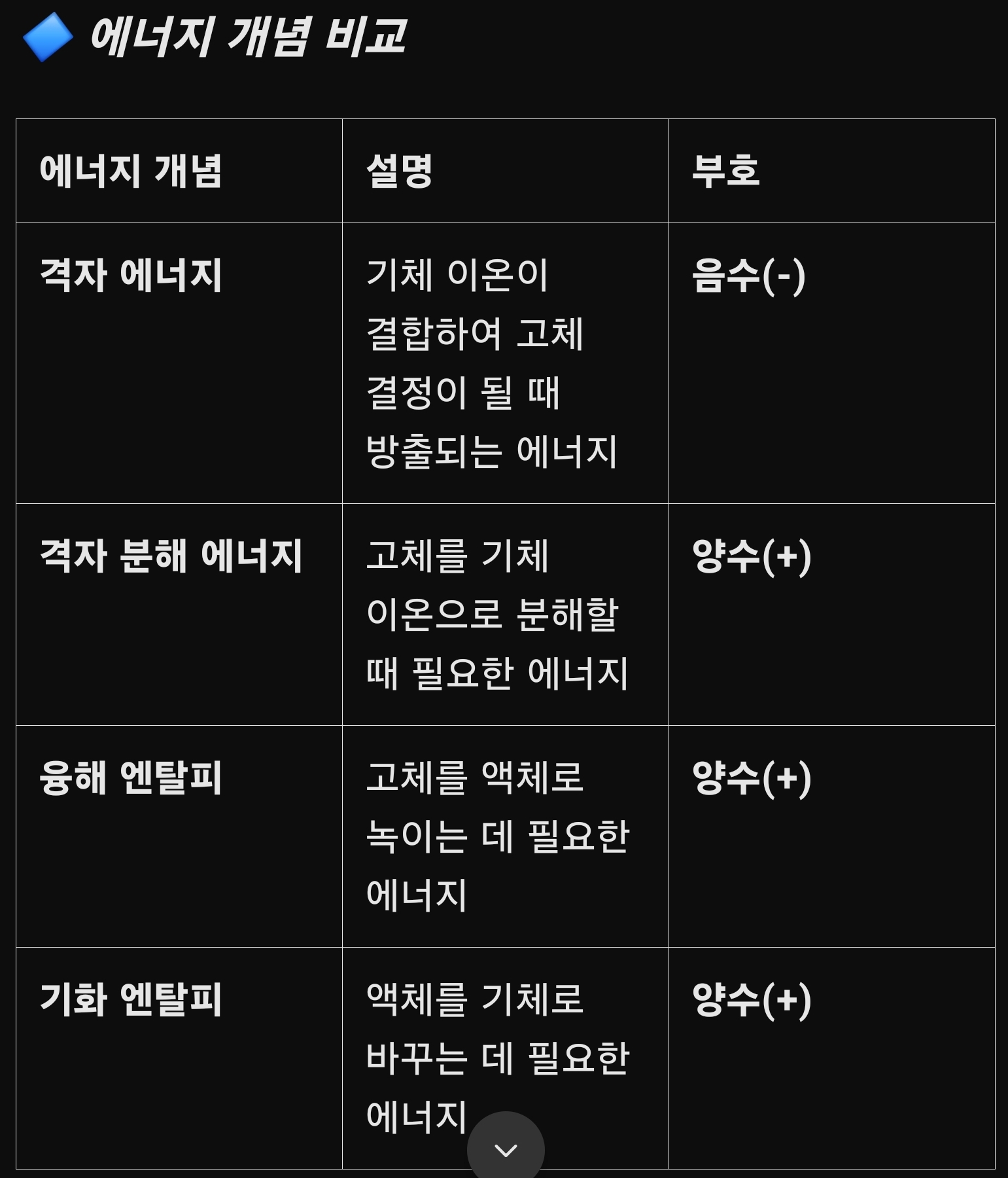
🔷 에너지 개념 비교
---
💡 결론
✔ 고체 NaCl을 액체로 만들 때 필요한 에너지는 "융해 엔탈피(Heat of Fusion)" 또는 "융해열"이라고 부릅니다.
✔ NaCl의 융해 엔탈피는 약 +27 kJ/mol이며, 이는 흡열 과정(에너지를 가해야 함)입니다.
✔ 이와 다르게, NaCl을 기체 상태로 만들 때는 더 큰 에너지(기화 엔탈피)가 필요합니다.
'공학' 카테고리의 다른 글
| 탄산염광물의 종류 (0) | 2025.02.27 |
|---|---|
| 원자가 결합을 형성할 때 형식 전하에 대한 만족이 중요하니 옥테트 룰에 대한 만족이 중요하니? (0) | 2025.02.26 |
| 아보가드로의 법칙(Avogadro's Law) 설명 (0) | 2025.02.24 |
| 확률계산시 두 사건이 and조건이면 각 사건의 발생확률을 서로 곱하고, 반면 or조건이면 서로 더한다 (0) | 2025.02.24 |
| 전 세계에 우리나라처럼 선 캄브리아 때부터 존재했었던 대륙은 어떤 것들이 있을까. 지역적 규모 등 (0) | 2025.02.23 |


댓글